您好!欢迎访问洛阳富道生物科技有限公司官方网站!
MSC的临床疗效,根植于其多向分化潜能、强大的免疫调节功能以及丰富的旁分泌效应。这些生物学特性统称为“干性”,是MSC作为治疗产品的灵魂。但在细胞工厂的规模化扩增过程中,细胞会经历“复制性衰老”,表现为增殖放缓、特定表面标志物丢失、分化能力减弱以及免疫调节因子分泌减少。如何在工业级放大过程中,设计出精妙的工艺路线,在收获海量细胞的同时,牢牢锁住其治疗潜能,是决定细胞治疗产品能否从实验室走向临床、从概念变为药品的生死线。本文将深入剖析MSC扩增中产量与干性的矛盾根源,并提供一套在细胞工厂中实现两者平衡的、可落地的综合策略与最佳实践方案。

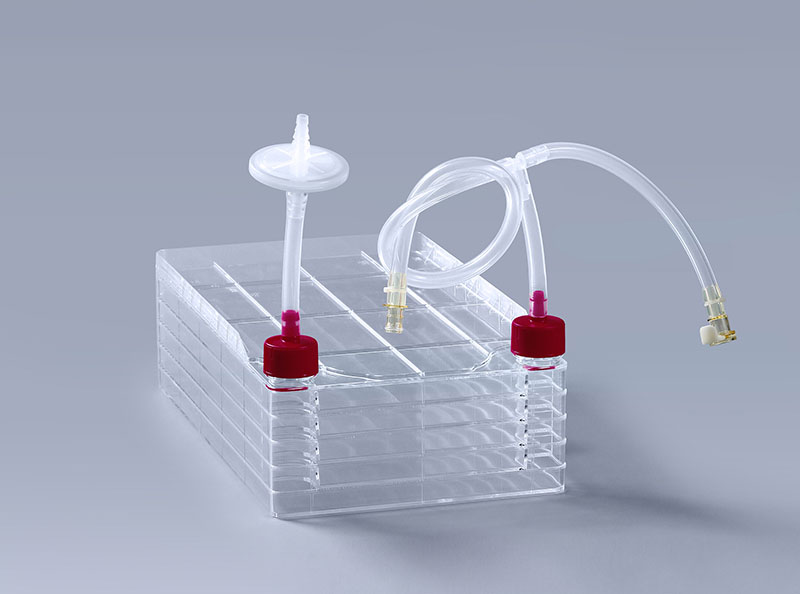
细胞工厂
核心矛盾:为何扩增会“稀释”MSC的干性?
在细胞工厂的多层表面进行高密度、多代次培养时,MSC面临多重应激压力,导致干性衰减:
复制性衰老:端粒随细胞分裂而缩短,触发p53/p21等衰老信号通路,使细胞周期停滞。
氧化应激累积:高代谢活性及培养环境中的活性氧(ROS)过量产生,损伤细胞DNA、蛋白质和脂质,加速衰老进程。
机械与接触抑制:细胞在工厂载体上铺满后,接触抑制信号增强,细胞骨架和核内基因表达谱发生改变,向分化或衰老状态倾斜。
微环境失衡:营养物质(如葡萄糖、谷氨酰胺)快速耗竭,代谢废物(乳酸、氨)大量积累,导致局部pH值、渗透压和溶氧剧烈波动,形成不利于干性维持的“毒性”微环境。
平衡策略一:优化培养基——构建维持干性的“营养基座”
培养基是决定细胞命运的化学微环境,其配方是平衡工艺的起点。
选用专用无血清培养基:避免使用含动物血清的培养基,其批次间差异大且成分不明。应选择化学成分明确、专为MSC设计的无血清/无异种培养基。这类培养基通常含有维持MSC干性所必需的特定生长因子、脂质和微量元素。
精准添加关键生长因子:
碱性成纤维细胞生长因子(bFGF):是维持MSC增殖和自我更新的核心因子。在培养基中持续补充5-10 ng/mL的重组人bFGF,可显著延缓细胞衰老,并维持多能性标志物(如Oct-4, Nanog, SSEA-4)的表达。
转化生长因子-β(TGF-β)超家族成员:如低浓度的TGF-β1或BMP-4,可在特定条件下促进MSC的自我更新而非分化。
强化抗氧化与抗衰老支持:
抗坏血酸(维生素C):作为强抗氧化剂和胶原合成辅因子,添加50-250 μM的维生素C可有效降低细胞内ROS水平,改善细胞外基质,为干性维持提供支持。
烟酰胺(维生素B3):作为NAD+的前体,有助于维持细胞能量代谢和sirtuin蛋白的活性,对抗衰老。
平衡策略二:革新培养工艺——实施动态精细的“过程控制”
在细胞工厂中,工艺参数的控制比在培养皿中更为关键,需要从静态思维转向动态管理。
接种密度的科学设定:采用相对较高的接种密度(如5,000-8,000 cells/cm²)进行传代。这能使细胞更快进入对数生长期,减少在低密度下的适应期和应激反应,有利于维持干性。避免为追求代次而进行极端稀释。
汇合度的精准把控——把握“黄金传代点”:这是平衡工艺中最关键的操作节点。严禁让细胞生长至完全汇合(100%)。应在细胞达到70-80%汇合度时立即进行传代。此时细胞处于旺盛增殖期,衰老通路尚未被大规模激活。建议使用实时在线显微镜或定期取样进行精准监控。
消化操作的温和化:使用低浓度胰蛋白酶(如0.05% Trypsin-EDTA)进行短时消化(通常室温2-3分钟),并立即用含血清或胰酶抑制剂的完全培养基中和。剧烈的消化会损伤细胞膜蛋白,影响其后续的贴壁、增殖和信号传导功能。
引入灌流培养模式:对于大规模生产,在细胞工厂中采用灌流培养是革命性的进步。通过持续移除废液并补充新鲜培养基,可以维持营养物质和代谢废物的稳态,为MSC提供一个更接近生理的稳定微环境,已被多项研究证实能更好地维持细胞干性、活率和功能。
平衡策略三:建立多维质量监控体系——用数据驱动决策
没有量化检测,就无法实现真正的质量控制。必须建立贯穿整个扩增过程的关键质量属性(CQA)放行标准。
身份鉴定(Identity):定期(如每2-3代)通过流式细胞术检测国际细胞治疗学会(ISCT)定义的最低标准:CD73、CD90、CD105阳性率>95%,CD34、CD45、HLA-DR阴性率<2%。
效力检测(Potency)——干性的核心衡量:
三系分化潜能:定期抽样进行成骨、成脂、成软骨诱导分化,并通过特异性染色(茜素红、油红O、阿尔新蓝)或qPCR检测标志基因表达,定量评估分化能力是否保留。
免疫调节功能:通过体外与活化外周血单个核细胞(PBMC)共培养实验,评估MSC对T细胞增殖的抑制率。或直接检测培养上清中吲哚胺2,3-双加氧酶(IDO)、前列腺素E2(PGE2)、白细胞介素-10(IL-10) 等关键免疫调节因子的分泌水平。
衰老与压力标志物监测:
β-半乳糖苷酶(SA-β-gal)染色:检测阳性细胞比例,这是细胞衰老的经典标志。
基因与蛋白水平:通过qPCR或Western Blot检测p16INK4a、p21等衰老相关基因的表达。
活性氧(ROS)检测:使用荧光探针(如DCFH-DA)检测细胞内ROS水平。
结论:迈向“质量源于设计”的MSC产业化生产
在细胞工厂中实现MSC产量与干性的平衡,标志着一场从“数量优先”到“质量优先”的范式转变。它要求开发者:
将干性维持作为工艺开发的北极星指标,而非事后的补救目标。
采用基于细胞生理反馈的动态过程控制策略,替代固定的、粗放的时间表。
建立以身份、纯度和效力为核心的多维、实时质量监控体系,确保每一批细胞产品都是疗效可预测的“活体药物”。
成功的平衡工艺,意味着您从细胞工厂中收获的不仅是符合数量要求的细胞,更是功能完备、治疗潜力明确、批次间稳定的高质量细胞治疗产品。这不仅是技术上的成功,更是确保患者安全与疗效、满足严格监管要求的基石。